9月6日,Ironwood公告宣布,其鸟苷酸环化酶C激动剂利那洛肽一项III期研究成功,治疗儿童功能性便秘(FC)患者。这是首款在III期研究中证明对儿童FC患者有效的药物。Ironwood表示,将与艾伯维共同推进该适应症的上市申请。

便秘是一种儿童时期常见的胃肠道疾病,其中FC约占儿童便秘的90%~95%,其临床表现为排便次数减少、排便不尽感和持续性排便困难。
利那洛肽是一款由Ironwood自主研发的鸟苷酸环化酶-C(GC-C)激动剂,于2012年8月首次获批上市,适应症为成人慢性特发性便秘(CIC)和便秘型肠易激综合征(IBS-C)。研究表明,其作用机制为:①利那洛肽结合并激活肠上皮细胞内的GC-C受体,导致肠液分泌增加、转运加速;②肠内痛觉神经活动减少,改善腹痛。
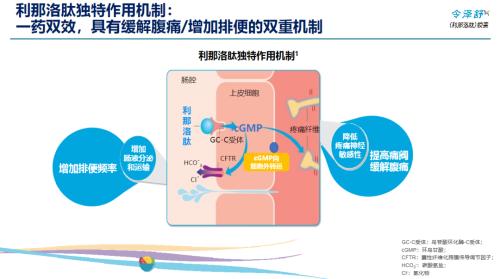
利那洛肽的作用机制(来源:阿斯利康PPT)
2009年11月,安斯泰来与Ironwood达成合作,获得利那洛肽在日本、印度尼西亚、菲律宾、中国台湾和泰国的独家开发和商业化权益。后来,阿斯利康和艾伯维相继与Ironwood达成合作,阿斯利康获得利那洛肽在中国(除了台湾)的独家开发、生产和商业化权益,艾伯维则获得利那洛肽在上述国家和地区以外的独家权益。
该研究是一项多中心、随机、双盲、平行组III期临床试验,共纳入330例患者,旨在评估利那洛肽治疗6-17岁儿童FC和IBS-C患者的疗效和安全性。其中FC患者接受每日1次72μg的利那洛肽,IBS-C患者接受每日1次145μg和249μg的利那洛肽。对FC患者来说,试验的主要终点为第12周时每周自发排便频率(SBMs频率/周)的变化;对IBS-C患者来说,试验的主要终点为12周内至少有6周达到腹痛及SBM(APS)+2应答的患者比例。APS+2应答指患者的SBMs频率/周至少增加2个单位和平均腹痛分数至少降低30%。
本次公布的结果为在FC患者人群中进行的部分。结果显示,利那洛肽可在统计学意义(p<;0.0001)和临床意义上改善SBMs频率/周。试验还达到了粪便硬度改善的次要终点(p=0.0001)。粪便硬度通过儿童大便分型量表(p-BSFS)评估。此外,利那洛肽具有良好的耐受性,其安全性也与既往在儿童FC和肠易激综合征患者中的研究一致。最常报告的治疗中出现的不良事件是腹泻,利那洛肽组的发生率为4.3%,而安慰剂组为1.8%。
Ironwood高级副总裁、首席医疗官兼研究和药物开发部负责人Mike Shetzline说:“我们对这项III期试验的结果感到兴奋,并专注于与我们的合作伙伴艾伯维一起确定一条快速的监管路径,以向有需要的6-17岁儿童患者提供这种潜在的首创FC疗法。”


- A股避雷针:金运激光实控人被判处有期徒刑四年,莫高股份董事长内幕交易被罚150万元
- 供需关系阶段性好转,生猪价格岁末年初涨近一成
- 脑机接口临床试验迎来重大突破,政策支持脑机接口设备将获优先审批
- 11家中国实体被列入实体清单,关注半导体设备国产化机会
- 雷鸟“联姻”阿里猛攻AI眼镜,2025年有望成为AI眼镜元年
- CES 2025即将开幕,AI与端侧设备结合值得期待,英伟达或宣布进军AI PC
- 微信“蓝包”扩大测试范围、推出激励计划,有望迎旺季催化
- 人民币汇率单边贬值风险总体可控,短期关注人民币贬值受益标的
- 央行例会释放政策新信号,Q1信贷投放力度或加码,优质银行股估值溢价有望重新回归
- 大基金三期迎来最新进展,豪掷1640亿元设立子基金!国产芯片将迎风口




